| Главная » Статьи » Кожные и венерические болезни |
Новые подходы к терапии герпесвирусной инфекции
|
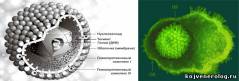
Вирусы, относящиеся к семейству Herpesviridae, принадлежат к числу возбудителей с большой социальной значимостью, что определяется не только широтой распространённости герпесвирусной инфекции (ГИ) и уровнем летальности, но и особенностями патогенеза ГИ, и разнообразием клинических проявлений. По мнению ВОЗ в настоящее время речь идёт о пандемии ГИ: от 65% до 90% взрослого и детского населения нашей планеты инфицировано герпесвирусами. При этом после первичного инфицирования в детском возрасте герпесвирусы могут пожизненно персистировать в организме человека, реактивируясь по истечении многих десятков лет. Пациенты, обладающие иммунной недостаточностью, имеют наиболее частые обострения герпетической инфекции. Интенсивное внедрение молекулярно-биологических методов в вирусологические и иммунологические исследования открыли новые возможности терапии герпесвирусной инфекции. Выяснение особенностей взаимодействия вируса и организма-хозяина, изучение механизмов, позволяющих вирусу избегать воздействие иммунной защиты, указывает реальный путь создания новых противовирусных препаратов. И эти пути поиска связаны не только с открытием новых химических препаратов, подавляющих репликацию вируса. Расшифровка иммунологических реакций, сопутствующих HSV-инфекции, позволяет определить наиболее существенные звенья иммунитета, воздействие на которые сделает реальным решить исход борьбы вирус-человек в сторону организма хозяина. Некоторые характеристики вируса простого герпеса В настоящее время семейство Herpesviridae включает 8 антигенных серотипов вирусов герпеса человека, которые распределены по трём подсемействам [Manual of Clin. Microbiol]: - Alfaherpesvirinae вирус простого герпеса 1 типа - ВПГ-1 (Herpes simplex virus тип 1 - HSV-1), вирус простого герпеса 2 типа - ВПГ-2 (Herpes simplex virus тип 2 - HSV-2), вирус ветряной оспы – опоясывающего лишая – ВВО-ОГ (Varicella-zoster virus – VZV), или вирус герпеса человека 3 типа - ВГЧ-3); - Betaherpesvirinae цитомегаловирус – ЦМВ (Cytomegalovirus – CMV), или вирус герпеса человека 5-го типа - ВГЧ-5, вирус герпеса человека 6 типа – ВГЧ-6 (Human herpesvirus 6 – HHV-6), вирус герпеса человека 7 типа – ВГЧ-7 (Human herpesvirus 7 – HHV-7); - Gammaherpesvirinae вирус Эпштейн-Барр – ВЭБ (Epstein-Barr virus – EBV) , или вирус герпеса человека 4 типа – ВГЧ-4 (Human herpesvirus 4 – HHV-4), вирус герпеса человека 8 типа – ВГЧ-8 (Human herpesvirus 8 – HHV-8), или вирус, ассоциированный с саркомой Капоши. Вирусы Herpes simplex (HSV-1 и HSV-2) подсемейства Alfaherpesvirinae (род Simplexvirus) характеризуются быстрым ростом и обладают одинаковым тропизмом как к эпителиальным, так и к нервным клеткам, который определяется наличием соответствующих клеточных рецепторов. Первичное заражение приводит к размножению (репликации) вируса в месте инвазии и сопровождается цитопатическим действием. Затем вирус перемещается либо по нервному стволу, либо распространяется гематогенным путём до нейронов региональных нервных ганглиев, где сохраняется в межрецидивный период (иногда на протяжении всей жизни человека), поддерживая латентную фазу ГИ. В момент реактивации вирус распространяется по нервным пучкам. Вирус герпеса относится к крупным (180-200нм) и сложноустроенным вирусам. Он состоит из трёх основных компонентов: нуклеоида, капсида и оболочки. Оболочка окружает икосоэдральный капсид (примерно 100 нм в диаметре), состоящий из 162 капсомеров. Между оболочкой и капсидом - слой белка, называемого тегументом. Нуклеоид расположен в центральной части и представляет собой геном вируса. HSV-1 и HSV-2 являются ДНК-содержащими вирусами и содержат линейную двуцепочечную ДНК, которая при инфицировании приобретает циклическую форму. Молекула ДНК вирусов представляет собой дуплекс, состоящий из двух ковалентно связанных компонентов – L и S, соединённых a-последовательностью [A. Dolan et al., 1999]. По концам L- и S-компонентов расположены инвентированные повторы. Геномы вирусов содержат около 85 открытых рамок считывания, пять из них – диплоидные (Рис. 1). Идентичность геномов HSV-1 и HSV-2 – более 80%. Кроме того, они характеризуются достаточной стабильностью, особенно в сравнении с некоторыми РНК-содержащими вирусами (HGV и HIV). Однако HSV-2 характеризуется более высоким уровнем мутирования, чем у HSV-1. При культивировании вируса в клеточных культурах для его воспроизводства достаточно участия половины генов, другая половина генома при репликации в таких идеальных условиях не востребована. Однако она оказывается совершенно необходимой при естественном инфицировании человека для преодоления защитных барьеров, избегания механизмов иммунной защиты, оптимизации репликации и распространения в организме человека. Репликация вируса начинается с его связыванием со специфическими клеточными рецепторами. При этом в процессе закрепления вируса на поверхности клетки и внедрения внутрь её используется пять гликопротеинов оболочки (Рис. 1). Следует заметить, что для контакта других вирусов используется значительно меньшее число гликопротеинов, например, у вируса гриппа – два, причём, для истинной адгезии необходим всего лишь один из них. Такое многообразие используемых гликопротеинов позволяет ВПГ инфицировать как эпителиальные (причём, различные типы эпителия), так и нервные клетки, различающихся по набору рецепторов [Spear P.G., 1993]. ВПГ может попадать в клетку не только через апикальный конец, но и в месте соединения клеток десмосомами, что обеспечивает ему возможность горизонтального распространения по эпителиальным клеткам. Это заведомо огромное преимущество для вируса, поскольку при таком пути распространения он избегает действия иммунных факторов защиты. Транскрипция вирусной ДНК происходит в ядре клетки при помощи РНК-полимеразы II хозяина. При этом транскрипция различных генов вируса зависит как от ядерных факторов клетки, так и от белков, закодированных в вирусном геноме. Имеются три главных класса генов, которые экспрессируются последовательно в течение литического цикла: альфа, бета и гамма, которым соответствуют сверхранние, ранние и поздние информационные РНК. Транслируемые в цитоплазме с этих иРНК белки имеют разные функции. Сверхранние – альфа-белки регулируют процессы транскрипции, а также участвуют в контроле синтеза ранних - бета-белков, они не обнаруживаются в зрелом вирионе. Бета-белки инициирует репликацию вирусной ДНК и участвуют в отключении синтеза альфа-белков. Поздние – гамма-белки являются структурными белками, участвующими в сборке вирусной частицы, на их долю приходится около 50% известных продуктов ВПГ. Гамма-гены подразделяются на гамма-1 гены, которые слабо экспрессируются до начала синтеза вирусной ДНК, и гамма-2 гены, экспрессия которых наблюдается только после начала синтеза ДНК [K.M. Khanna et. al., 2004]. Возможность существования в латентном состоянии является принципиальной особенностью вируса герпеса. Персистируя в нервных ганглиях, он использует естественные барьеры организма, защищающие нервную систему от иммунной интервенции. Переходя в латентное состояние, вирус пытается уйти от эффекторных иммунных механизмов. Это непродуктивная инфекция, в ходе которой в клетке при сохранении вирусного генома не образуются инфекционные вирионы. Динамика латентной инфекции проявляется в виде стадий становления, поддержания и реактивации. При репликации в эпителиальных клетках вирусные частицы достигают локальных нервных окончаний и транспортируются ретроградно от аксонов к ядрам нейронов в пределах сенсорного ганглия. Краткий период репликации HSV в некоторых сенсорных ганглиях сопровождается становлением скрытой (латентной) инфекции, итог которой - выключение репликативной функции вируса в нервных клетках. Механизм перехода в латентное состояние ВПГ изучен недостаточно. На следующем этапе поддержания латентной инфекции вирусный геном сохраняется в ядрах нейронов в виде циклической эписомы, в формировании которой участвуют гистоны клетки. Применение молекулярных методов исследования позволило выявить семейство РНК, транскрибирующихся в латентном состоянии, которые были названы LAT-транскриптом [G.C. Perng et al., 2000]- latency-associated transcript (Рис. 2). Одна из функций LAT-гена состоит в защите инфицированных нейронов от апоптоза. В частности, при инфицировании кроликов вирусом с делецией по LAT наблюдали увеличение апоптоза нейронов тройничного узла. В исследованиях N.W. Fraser было обнаружено, что часть LAT-гена HSV-1 участвует в образовании miRNA (микроРНК), которые в клетках исполняют роль важного механизма, контролирующего генную экспрессию [A. Gupta et al., 2006]. Подавление апоптоза достигается благодаря тому, что молекулы miRNA связываются со специфическими последовательностями информационной РНК двух генов, контролирующих апоптоз - TGF-b и SMAD-3, вызывая тем самым деградацию иРНК, и процесс трансляции этих белков не происходит. В результате латентно инфицированные нейроны не погибают, поддерживая тем самым существование вируса. При исследовании латентно инфицированных сенсорных ганглиев мышей были выявлены транскрипты сверхранних альфа-генов (ICP4), ранних бетта-генов (ICP8, ген тимидин киназы), которые транскрибируются до начала репликации ДНК [A.A. Nash, 2000]. Обнаружение этих транскриптов позволило предположить, что, находясь в латентном состоянии, вирус «не молчит», а все время пытается себя воспроизвести. Но на стадии включения гамма-2 генов, экспрессия которых необходима для начала синтеза ДНК, происходит блокировка списывания, транскрипция прекращается, и репликации вируса не происходит. Таким образом, при персистировании вируса реально работают механизмы, сдерживающие реактивацию HSV-инфекции. Взаимодействие иммунной системы и HSV-инфекции Исход заболевания при инфицировании вирусом герпеса зависит от возможностей организма воздействовать на различные проявления HSV-инфекции: патогенез HSV-инфекции, репликация вирусных частиц, распространение вируса от места его инокуляции, формирование латентной HSV-инфекции и её реактивация. Чувствительность к HSV-инфекции. Популяционные наблюдения клиницистов и эпидемиологов указывают на наличие генетического разнообразия как по чувствительности к HSV-инфекции, так и по вероятности её рецидивирования. Исследования, проведённые C. Lopez в 80-х годах прошлого столетия на инбредных линиях мышей, продемонстрировали, что чувствительность к HSV-инфекции может существенно различаться, и она непосредственно зависит от эффективности работы защитных механизмов врождённого иммунитета организма. На модели офтальмогерпеса было показано, что инфицирование HSV мышей чувствительной линии приводило к развитию тяжёлого энцефалита (у нормальных мышей развивался офтальмогерпес). Кроме того, нарушение естественного иммунитета у мышей приводило к развитию заболевания даже в том случае, когда их инфицировали мутантным штаммом HSV, на который нормальные мыши не реагировали. Дальнейшие исследования в этом направлении [W.P. Harford et al., 2004] подтвердили наличие наследственной составляющей, контролирующей чувствительность к HSV-инфекции посредством различных иммунных механизмов (Рис. 3). Нарушение какого-либо из перечисленных факторов [B.T. Rouse, M. Gierynska, 2001] приводит к повышению восприимчивости к инфекции и более тяжелому течению заболевания. Механизмы адаптивного иммунитета. Реакции адаптивного иммунитета контролируют как острую, так и латентную фазу HSV-инфекции (Рис. 4). Большой вклад в изучение иммунных механизмов, сдерживающих процесс реактивации герпесвирусной инфекции, внесли исследования на модельных объектах, которые позволили установить решающую роль цитотоксических Т-лимфоцитов [T. Liu et al., 2000]. Активация CD8+ Т-клеток, присутствующих в сенсорных ганглиях, определяется вирус специфическими антигенами, которые ограниченно экспрессируются в латентно инфицированных нейронах. Эти CD8+ клетки образуют с нейронами синаптические структуры и способны блокировать реактивацию HSV в ex vivo культуре ганглиев. При этом введение антител против CD8+ приводит в культуре к усиленной реактивации вируса [T. Liu et al., 2000]. К настоящему моменту установлен один из факторов, обеспечивающих защитный противовирусный эффект по отношению к нейронам. Он опосредуется γ-интерфероном, который синтезируется CD8+ Т-клетками [T. Liu et al., 2001; V. Decman, et al., 2005]. Имеющиеся данные позволяют предполагать, что γ-интерферон может оказывать подавляющий эффект на различные ступени процесса реактивации, которые необходимы для включения γ-2 генов. Если непосредственно к нервным клеткам приближены цитотоксические, то далее располагаются хелперные Т-лимфоциты. Последние синтезируют цитокины, которые стимулируют продукцию цитотоксическими клетками γ-интерферона и таким образом помогают CD8+ Т -лимфоцитам в выполнении их функции. Таким образом, если цитотоксические лимфоциты находятся в хорошем функциональном состоянии и продуцируют высокое количество гамма-интерферона, то вирус не может начать репликацию. При любых воздействиях, приводящих к подавлению функции Т-клеток, вирус реактивируется. Эксперименты на модели стресса латентно инфицированных мышей с успехом это подтвердили. У мышей, подвергнутых физическому стрессу (мыши усиленно бегали), наступала активная фаза инфекции, при этом реактивация вируса коррелировала с ингибицией продукции гамма-интерферона. И, наконец, необходимо отметить, что, подавляя активность вируса, CD8+ Т-клетки не проявляют свою потенциальную цитолитическую активность по отношению к нейронам. Указанное ингибирование киллерной активности CD8+ Т-клеток достигается при взаимодействии рецептора CD94-NKG2a, экспрессирующегося на их поверхности, с лингандой Qa-1b, присутствующей на большинстве нейронов [S. Suvas et al., 2006]. Таким образом, сдерживание латентной HSV-инфекции или реактивация вируса непосредственно зависит от функционирования цитотоксических Т-лимфоцитов и Т-хелперов первого типа, которые их поддерживают. Дендритные клетки. Дендритные клетки (ДК) играют ключевую роль на пересечении путей врождённого и адаптивного иммунитета. Располагаясь повсеместно в теле, ДК участвуют в распознавании как собственных, так и чужеродных антигенов и способствуют развитию протективного иммунитета либо толерантности. Любой из этих процессов опосредуется различными классами консервативных рецепторных структур (Рис.5), включающими, прежде всего, Toll-подобные рецепторы (TLR - Toll-like receptors) и лектиновые рецепторы С-типа (CLR – C-type lectin receptors). Если TLR характеризуются как ключевой элемент распознавания «чужого», то семейство CLR участвует ещё и в распознавании аутоантигенов с последующим развитием толерантности к ним. При этом контроль аутотолерантности осуществляется за счёт индукции Т-регуляторных клеток (Treg) [B.A. ′t Hart and Y.van Kooyk, 2004]. Баланс между стимуляцией через TLR и CLR имеет большое значение для инициации функций дендритных клеток. Интеграция сигналов TLR и CLR может иметь различные исходы в зависимости от конкретного сочетания рецепторов. В результате возможно подавление созревания ДК, изменение спектра продуцируемых ими цитокинов, а также модуляция иммунных реакций с преобладанием Th1 или Th2 ответа [C-H. Chen et al., 2006]. Кроме того, в ряде случаев вирусы взаимодействуют с CLR на зрелых и незрелых ДК, в которых затем происходит интернализация вируса. Защищённый таким образом от деградации вирус затем может передаваться Т-клеткам при их контакте с ДК [N. Teleshova et al., 2003; S. Peretti et al., 2005]. Такая трансмиссия вируса приводит к появлению популяции инфицированных Т-клеток. Эти инфицированные клетки становятся объектами для распознавания цитотоксическими лимфоцитами, которые вместо того, чтобы блокировать источник вирусной инфекции в эпителии, реагируют на ближайшее Т-клеточное окружение. В результате такого распознавания иммунная система оказывается практически с выключенным адаптивным иммунным ответом (Рис. 6). Особое значение в развитии противовирусного врождённого иммунитета принадлежит плазмоцитоидным дендритным клеткам, производящим интерфероны I-го типа. Это Natural Interferon-Producing Cells – NIPC – естественные клетки, продуцирующие интерферон [F.P. Siegal et al., 1999; N. Kadowaki et al., 2000; K. McKenna et al., 2005]. В исследованиях in vitro было показано, что HSV-1 активирует NIPC через систему, в которой участвует TLR9 и адапторная молекула MyD88, передающая сигнал внутрь клетки [A. Krug et al., 2004]. Производя интерфероны α и β в количестве, в 1000 раз большим, чем другие клетки крови, они непосредственно подавляют репликацию вируса. Вторая не менее важная функция этих клеток состоит в инициации и направлении адаптивного вирус специфического иммунитета. Натуральные киллеры. Огромную роль в противовирусной защите играют естественные киллеры, активизирующиеся на самых ранних этапах инфекции до появления вирус специфических CTL и антител. Протективный иммунный ответ опосредуется NK-клетками перфорин-зависимым лизисом и продукцией цитокинов. Активность натуральных киллеров контролируется различными активирующими и ингибирующими рецепторами и ко-рецепторами, соединение которых с различными лигандами, присутствующими на поверхности клеток-мишеней, генерирует активирующие или ингибирующие сигналы NK-клеткам. Генетическая запрограммированность чувствительности к герпесвирусной инфекции была продемонстрирована в исследованиях на мышах. Белок m157 продуцируется мышиным цитомегаловирусом и определяет чувствительность вирус инфицированных клеток к NK-опосредованному лизису (Рис.7). Этот белок может связываться с двумя NK-клеточными рецепторами Ly49H и Ly49I. Ly49H является активирующим клеточным рецептором, а Ly49I обладает ингибирующим эффектом [Ianello et al., 2006]. Присоединение m157 к Ly49H генерирует активационный сигнал, который передаётся внутрь клетки адапторным белком. В результате происходит высвобождение перфорина и последующая гибель инфицированной клетки. Такая ситуация свойственна линиям мышей, устойчивым к MCMV-инфекции. Но у чувствительных к вирусной инфекции линий мышей активационный сигнал и соответственно высвобождение перфорина NK-клетками отсутствует, и лизис инфицированных клеток не происходит. Это может возникать по нескольким причинам: могут либо вообще отсутствовать распознающие рецепторы (линия BALB/c), либо соединение с другими адапторными молекулами приводит к передаче в клетку ингибиторного сигнала (линия 129/J). Способность к презентации. Сопряжённая эволюция вирусов и их хозяев привела к развитию различных механизмов защиты от вирусной инвазии, с одной стороны, и изощрённых способов избегания антивирусного иммунитета, с другой [A. Ianello et al., 2006]. Вирус специфические CTL узнают вирусные антигенные пептиды в ассоциации с антигенами MHC I класса, которые присутствуют на всех клетках организма. Снижение экспрессии этих антигенов на поверхности инфицированных клеток предотвращает их узнавание и соответственно последующий киллинг. Эта способность блокировать или снижать уровень экспрессии молекул главного комплекса гистосовместимости MHC I широко распространена среди представителей семейства Herpesviridae. Для этого используются различные механизмы (Рис. 8). В настоящий момент наибольшее их разнообразие выявлено для цитомегаловируса, у которого даже имеется уникальный регион в геноме, кодирующем не менее четырёх белков. Некоторые из упомянутых способов связаны с блокированием функции гетеродимерного комплекса TAP – transporter associated with antigen processing - (ТАР-1 и ТАР-2), обеспечивающего транслокацию пептидов после протеасомной деградации в эндоплазматический ретикулум, или тапазина, формирующего контакт между МНС I и ТАР. Такое ингибрование, обеспечиваемое белком ICP47 у HSV-1 и белком U56 у HCMV, приводит к нарушению сворачивания молекулы MHC I и её экспрессии на клеточной поверхности. В других случаях белок (US2 HCMV) связывается с молекулой МНС I при гликозилировании, что приводит к ретроградному транспорту комплекса в цитоплазму с последующей деградацией. Белок US11 HCMV индуцирует быструю деградацию молекулы МНС I при её синтезе. Следствием ассоциации белка US3 HCMV с одной из цепей МНС I является возвращение комплекса в эндоплазматическую сеть, что лишает его необходимых взаимодействий и созревания. Семейство белков К3 гамма-вирусов обладает убиквитин-лигазной активностью, они подавляют поверхностную экспрессию гликопротеинов, в частности, тяжёлой цепи MHC I класса, способствуя убиквитин опосредованной протеасомной деградации. Кроме того, многие вирусы используют стратегию избирательного воздействия на различные молекулы MHC I. Так они подавляют экспрессию аллелей HLA-A и –В, которые представляют вирусные эпитопы для CTL, не влияя на экспрессию аллелей HLA-C и HLA-E.  Цитотоксические лимфоциты. CD8+ CTL участвуют в контроле как острой, так и латентной HSV-инфекции. Отсутствие Т-клеточного иммунитета сопровождается бесконтрольной репликацией вируса и завершается развитием энцефалита и гибелью экспериментальных животных [A. Lang et al., 2005]. Активация Т-клеток в дренирующих лимфоидных органах приводит к появлению новых вирус специфичных CD8+ Т-лимфоцитов. В результате их пролиферации формируется популяция специфичных эффекторных клеток, которая распространяется по лимфоидной ткани. При этом в начале иммунного ответа часто наблюдают фазу апоптоза других предсуществующих в лимфоузлах Т-клеток, особенно вирус неспецифичных (Рис 10). Такой своеобразный физиологический ответ лимфоидной ткани диктуется необходимостью реализации нового иммунного ответа. Вторая волна апоптоза CD8+ T-клеток наблюдается при терминации иммунного ответа [M. Pellegrini et al., 2003]. Тесная связь пролиферации и апоптоза осуществляется как на клеточном, так и на популяционном уровнях, и в поддержании баланса между проапоптотическими и антиапоптотическими факторами участвуют цитокины. Вирусы обладают различными механизмами, способными влиять на эти жизненно важные процессы путём уменьшения количества CTL или снижения их активности [M.J. Raftery et al., 1999; C.M. Jones et al., 2000; D.D. Sloon et al., 2003; M. Pellegrini et al., 2003], что позволяет вирусу уйти от эффекторных механизмов иммунитета. А наблюдаемое снижение количества CTL приводит к формированию лейкопении у пациентов с HSV-инфекцией. Участие интерлейкина-2 в обеспечении протективного иммунитета при HSV-инфекции По мере получения новых данных наши представления о роли интерлейкина-2 в различных иммунологических реакциях уточняются. Всемирно известно, что этот цитокин является продуктом, преимущественно Th1 CD4+ лимфоцитов (90%), а также цитотоксических CD8+ лимфоцитов (10%). Обладая относительно узким спектром мишеней, несущих рецептор для IL-2 на своей поверхности, IL-2 способен поддерживать пролиферацию Th1, NK, CTL и В-лимфоцитов (Pис. 10). Воздействуя на моноциты, IL-2 усиливает генерацию активных форм кислорода и перекисей. При этом цитокиновая регуляция функций клеток-мишеней IL-2 осуществляется по аутокринному и паракринному механизмам. Пролиферативная активность IL-2 в отношении NK и CTL, а также его способность активировать макрофаги, необходимые при острой фазе вирусной инфекции, демонстрирует нам, что этот цитокин поддерживает те же реакции, которые являются защитными при вирусном иммунитете. Биологическая активность IL-2 связана с его взаимодействием со специфическими рецепторами, которые экспрессируются клетками-мишенями на своей мембране. В состав рецепторов IL-2 входят три цепи: две цепи - IL2R-α (CD25, p55) и IL2R-β (CD122, p75) работают в качестве связывающего лиганда, а третья цепь IL2R-γ (CD 132, p64) обеспечивает проведение сигнала. Сочетание указанных цепей приводит к формированию рецепторов разной афинности. Рецептор низкой афинности состоит только из легкой цепи IL2R-α. Рецептор промежуточной афинности содержит две цепи - IL2R-β и IL2R-γ. Высокоафинный рецептор состоит из 3-х цепей. Комплекс IL-2 с высокоафинным рецептором поглощается клеткой (интернализутся). После этого следует каскад реакций, который обеспечивает передачу сигнала от клеточной поверхности к ядру посредством взаимодействия тирозиновых киназ семейства JAK с внутриклеточными сигнальными компонентами STAT-белками. Активированные STAT-белки транслоцируются в ядро, где они связываются с определёнными последовательностями ДНК [C. Schindler and J.E. Darnell, 1995; V. Imbert et al., 1999]. После воздействия IL-2 на активированную клетку-мишень уже через 4 часа в ядре обнаруживается изменение экспрессии более 72 известных уникальных генов, которые кодируют клеточные мембранные белки и рецепторы, продукцию медиаторов и цитокинов, метаболизм и биосинтез, регуляторов клеточного цикла и транскрипции [Carol B. and Kendall A.S., 2002]. Регуляция на молекулярном уровне обеспечивает реализацию различных проявлений жизнедеятельности клеток - пролиферации, выживания, дифференцировки, функциональной активности (Рис. 11). Взаимодействие IL-2 с IL-2R лежит в основе развития эффективного Т-клеточного ответа, который обеспечивает защиту от вирусной инфекции и лежит в основе терапевтического применения препаратов IL-2 (Рис. 12). Процесс, приводящий к интенсивной клональной Т-клеточной экспансии, проходит многоэтапно в соответствии с поступлением трёх сигналов, в результате чего наивные Т-клетки дифференцируются в эффекторные Т-клетки, участвующие в противовирусной защите. Инициация протективного иммунитета начинается со взаимодействия Т-клеточного рецептора с антиген презентирующими клетками (сигнал 1). Следующий этап требует костимуляции (CD28 и CD40), при отсутствии которой наступает анергия Т-клеток (сигнал 2). Активация Т-клеток и ранняя стадия пролиферации связана с появлением IL-2R, к которому присоединяется IL-2, продуцируемый наивными Т-клетками. Пролиферация активированных Т-клеток приводит к дальнейшему накоплению клона – так осуществляется интенсивная клональная экспансия. In vitro этого можно достигнуть с помощью IL-2, а in vivo, кроме интерлейкина-2, для поддержания процесса требуются и другие цитокины. Исследования последних лет показали, что участие IL-2 необходимо уже на самых ранних стадиях развития иммунного ответа, сопряжённых с участием дендритных клеток. Как уже было указано ранее, дендритным клеткам принадлежит решающая роль в инициации иммунного ответа (Рис. 13). Двойственная роль ДК проявляется в их способности активировать как врождённый, так и адаптивный иммунитет[E. Klechevsky et al., 2005]. Ранняя активация ДК под действием вирусной инфекции стимулирует синтез различных цитокинов, в том числе и IL-2, что приводит к активации NK и тем самым способствует ограничению распространения вируса уже на самым ранних стадиях инфекции [D.H. Raulet, 2004; S.H. Kassim et. al., 2006]. Одновременно происходит перестройка актинового цитоскелета, что сопутствует последующим процессам созревания ДК и их миграции в лимфоидные органы, где ДК начинают активно работать как лимфоидная популяция [G.Pollatra et al., 2003; T.R. Mempel et al., 2003; H. Yoneyama et al., 2005]. Формируются иммунологические синапсы между ДК и Т-клетками и происходит примирование CD4+ и CTL клеток (Рис. 14), и все эти процессы происходят при участии IL-2. Таким образом, исследования последних лет, выявившие участие IL-2 в процессах примирования CD4+ Т-клеток и CTL, поддержания ранних этапов пролиферации лимфоцитов, а также в активации NK, указывают на ключевую роль IL-2 на ранних стадиях развития иммунного ответа. Полученная информация открывает новую возможность применения лечебных препаратов IL-2 уже с самого раннего момента активации инфекции. Более глубокое рассмотрение популяции NK-клеток показало, что два фенотипически различающихся NK типа - СD16++CD56- и СD16-CD56++ - локализуются в разных структурах организма и выполняют разные функции (Рис. 15). СD16++CD56- являются эффекторными клетками, отвечающими за киллинг инфицированных клеток посредством использования перфоринов и гранзимов. А клетки СD16-CD56++ выполняют преимущественно регуляторные функции и способны к синтезу большого количества гамма интерферона. Активируясь под влиянием вируса, они по лимфатическому сосуду попадают в лимфоузел. Синтезируемый NK гамма-ИФН способствует процессингу и презентации антигена Т-клеткам и влияет на поляризацию Т-клеточного ответа, способствуя дифференцировке Т-хелперных клеток 1 типа. При этом активация NK СD16-CD56++ на ранней стадии иммунного ответа происходит при контакте с дендритными клетками и зависит от IL-2, который они продуцируют (Рис.16). Образующийся иммунологический синапс NK-ДК характеризуется взаимообменом цитокиновыми сигналами: интерлейкиновый (IL-2) сигнал исходит от дендритных клеток и способствует активации NK, а гамма-ИФН, продуцируемый активированными NK, поддерживает дендритные клетки. На поздней стадии иммунного ответа межклеточные контакты формируется между NK, ДК и Т-хелперами также за счёт обмена цитокиновыми сигналами, и здесь IL-2 является важнейшим участником этих межклеточных взаимоотношений (Рис. 16). Таким образом, можно заключить, что IL-2 является важнейшим цитокином, который участвует в активации Т-лимфоцитов, дендритных клеток и НК клеток и проявляет свой эффект как на ранних, так и на поздних стадиях иммунного ответа.
ещё по теме рассказать друзьям | |
| Просмотров: 4656 | Теги: | Рейтинг: 0.0/0 |
| Всего комментариев: 0 | |